Movilización completa del ángulo esplénico del colon. Simulación en modelo cadavérico aplicada al abordaje quirúrgico ![]()
Javier Chinelli, Eduardo Olivera, Gustavo Rodriguez
Clínica Quirúrgica 2, Hospital Maciel. Montevideo, Uruguay.
Javier Chinelli
jchinelli01@gmail.com
Javier Chinelli: 0000-0002-3387-7365
Eduardo Olivera: 0000-0002-1396-5771
Gustavo Rodriguez: 0000-0003-3465-8364
El autor declara ausencia de conflictos de interés.
Recibido: junio de 2021. Aceptado: agosto de 2021.
Palabras clave: Ángulo esplénico; Movilización completa; Abordaje quirúrgico
ABSTRACT
Introduction: Complete splenic flexure (SF) mobilization is a complex technique with a steep learning curve.
Methods: An anatomic study of the SF and its different approaches was conducted on a cadaver-based simulated model. Surgical technique with laparoscopic medial approach is shown.
Results: Five different approaches were identified: anterior trans-omental, anterior, lateral, medial infra-mesocolic and medial trans-mesocolic approach. Fixating ligaments, SF vascular anatomy and main anatomic relationships are described.
Discussion: Surgeons must know the anatomy, relationships and approaches to the SF. With cadaveric simulation we were able to reproduce a previously validated teaching and training model to achieve a complete SF mobilization.
Conclusions: Cadaver-based simulated model of complete SF mobilization is a helpful tool applied to surgical practice.
Keywords: Splenic Flexure; Complete Mobilization; Surgical Approach
INTRODUCCIÓN
El ángulo esplénico (AE) del colon es una zona de especial complejidad anatómica como consecuencia del desarrollo embriológico.1 Su abordaje quirúrgico constituye una de las situaciones más desafiantes que se presentan en la cirugía colorrectal, en particular a causa del riesgo de lesión pancreática y/o esplénica.2
Su movilización puede ser parcial o completa, dependiendo de la patología a tratar. En este caso nos referiremos únicamente a situaciones que requieren una movilización completa, sea porque es necesaria su resección en caso de patología oncológica a dicho nivel, o bien su descenso para confeccionar una anastomosis colorrectal o coloanal sin tensión.3
Clásicamente se han descrito 3 abordajes para movilizarlo (anterior, medial y lateral) según la vía de acceso a la transcavidad de los epiplones o bursa omentalis4 y, recientemente, García-Granero et al.5 postulan 5 abordajes posibles en función de algunas modificaciones a los anteriormente mencionados. En Uruguay, una de las principales contribuciones al conocimiento de esta región anatómica y sus implicancias en el tratamiento de la patología neoplásica fue realizada por el Dr. Luis Praderi.6
Todo cirujano colorrectal debe conocer y poder enseñar estas alternativas técnicas, independientemente de que se utilice una vía de abordaje a la cavidad peritoneal laparotómica o laparoscópica. En cualquiera de estos escenarios, sea aprendizaje, entrenamiento y/o enseñanza, la simulación constituye una herramienta de capital importancia. Concretamente, el modelo en cadáver ofrece una gran fidelidad dada la posibilidad de reproducir exactamente la anatomía humana.7
El objetivo de este trabajo fue realizar un estudio anátomo-quirúrgico descriptivo del AE, describir los distintos abordajes para efectuar su movilización completa y analizar su utilidad aplicada a la práctica quirúrgica. Para ello, se utilizó un modelo de simulación en cadáver humano.
MATERIAL Y MÉTODOS
El material cadavérico humano utilizado fue obtenido por el Departamento de Anatomía de la Facultad de Medicina (Universidad de la República), de acuerdo con las normas que regulan la donación de cuerpos para investigación médica y educación.
La técnica de fijación y conservación cadavérica consistió en la inyección y recuperación de solución de formalina mediante abordaje femoral.
Se obtuvo la aprobación del Comité de Ética de la institución (Hospital Maciel).
Técnica de disección cadavérica
Tras acceder a la cavidad peritoneal se identificaron y seccionaron todos los ligamentos de fijación, señalando las principales relaciones anatómicas de interés y describiendo todas las posibles vías de acceso a la transcavidad de los epiplones.
Se realizó la disección completa de todo el mesocolon, desde el origen de los vasos cólicos medios, hasta la arteria hemorroidal superior, identificando todas las estructuras vasculares del mismo.
Se consideró como el espacio avascular del ángulo esplénico (EAAE) al área cuyos límites son: posteroinferior, el borde anterior o ventral del páncreas; anterosuperior, la arcada vascular más próxima a este último; medial, la rama izquierda de la arteria cólica media; lateral, la rama ascendente de la arteria cólica izquierda.
Técnica quirúrgica (ver video)
Se presenta la movilización completa del AE por vía laparoscópica, con abordaje inicialmente medial.
El paciente se coloca en posición de decúbito dorsal con anti-Trendelenburg y lateralización a la derecha. Se utilizan 4 trócares: uno de 10 mm periumbilical, dos de 12 mm en flanco derecho y paraumbilical izquierdo y uno de 5 mm en flanco izquierdo. El cirujano se sitúa a la derecha del paciente, el 1er ayudante (cámara) a su lado y el 2do ayudante a la izquierda del paciente.
Se incide el peritoneo paraaórtico por detrás de la vena mesentérica inferior (VMI), disecando la fascia de Toldt izquierda, identificando el uréter y los vasos gonadales, elevando el mesocolon y dejando por detrás la fascia pararrenal de Gerota. Se seccionan la arteria cólica izquierda (ACI) en su origen, así como la VMI a este mismo nivel y nuevamente debajo del borde inferior del páncreas. Luego se secciona el ligamento gastrocólico avanzando hacia la izquierda, hasta llegar al límite lateral de la bursa omentalis correspondiente al ligamento esplenocólico. Por último, se continúa la liberación seccionando los ligamentos parietocólico y frenocólico, hasta obtener una movilización completa del AE.
RESULTADOS
Disección cadavérica
Tras la disección se identificaron las siguientes estructuras ligamentarias de fijación:
En cuanto a los posibles abordajes para movilizar completamente el AE, se realizó una simulación de acceso a la transcavidad de los epiplones, encontrando 5 posibles formas de hacerlo (Fig. 1):
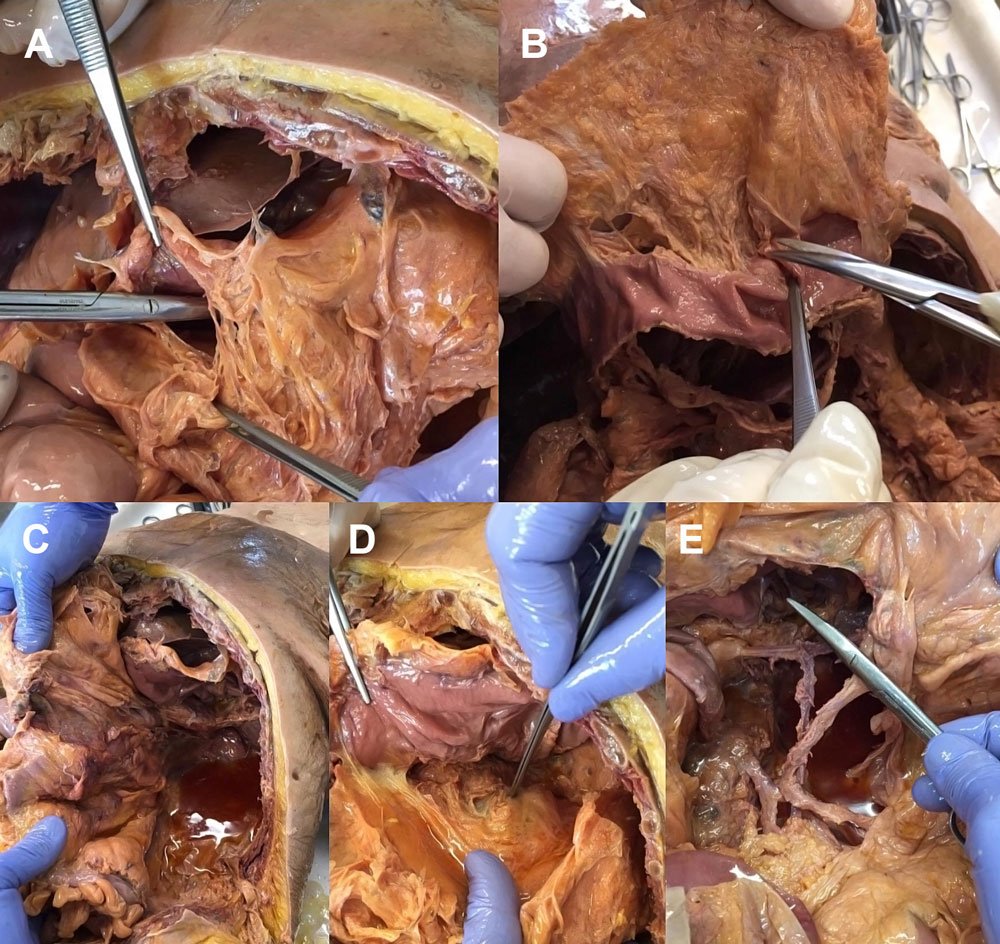
Figura 1 (A-E): Simulación de los 5 abordajes para acceder a la transcavidad de los epiplones (ver texto).
Tras la disección del mesocolon, se reconocieron las siguientes estructuras vasculares (Fig. 2):
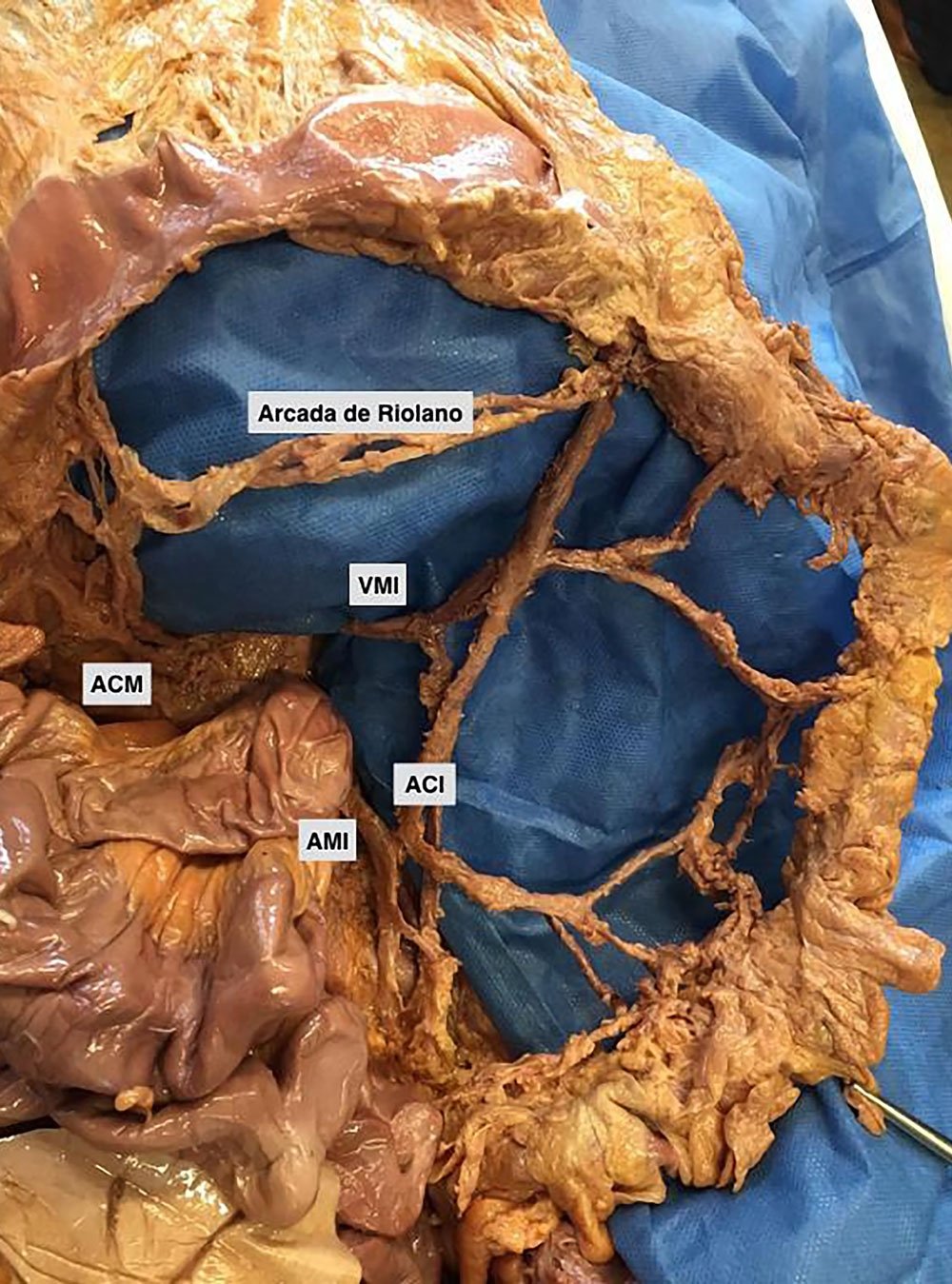
Figura 2: Anatomía vascular del ángulo esplénico.
ACM = arteria cólica media; VMI = vena mesentérica inferior; ACI = arteria cólica izquierda; AMI = arteria mesentérica inferior

Figura 3: Espacio avascular del ángulo esplénico.
En las Figs. 3 y 4 pueden observarse las relaciones anatómicas que el AE mantiene hacia atrás con el cuerpo y cola del páncreas, polo inferior del bazo, fascia de Gerota, uréter y vasos gonadales izquierdos. También el área denominada espacio avascular del ángulo esplénico (EAAE).
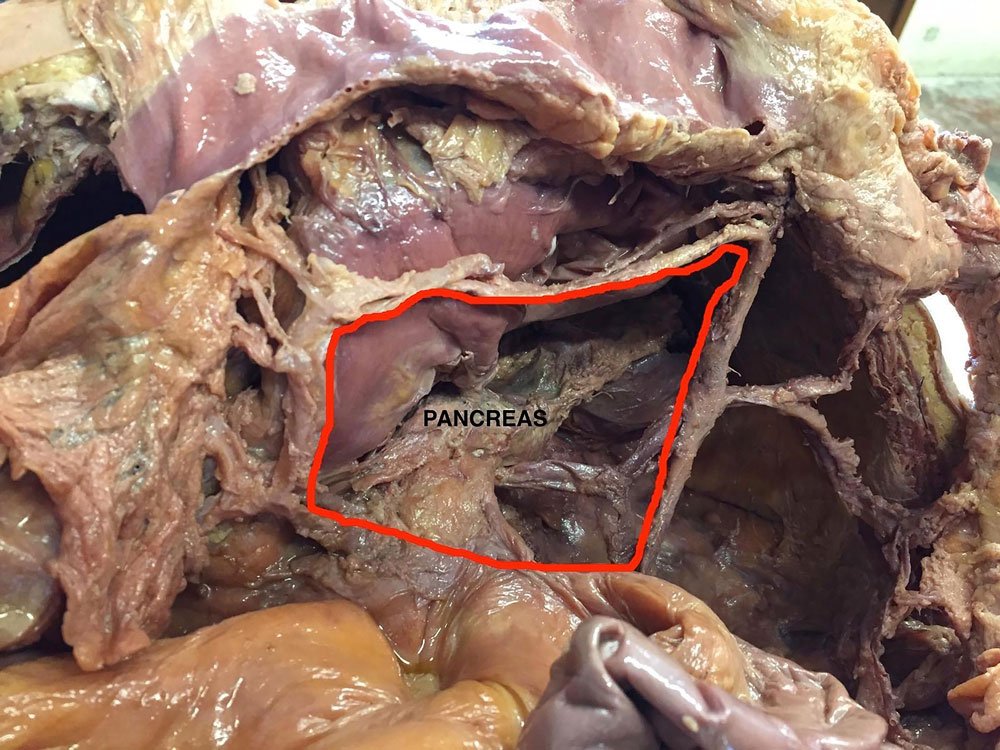
Figura 4: Relaciones posteriores del ángulo esplénico.
Técnica quirúrgica (video)
En el video pueden observarse todos los pasos de la técnica quirúrgica de movilización completa del AE precedidos de la disección cadavérica.
DISCUSIÓN
El abordaje quirúrgico del AE constituye un desafío por varios motivos, entre los que destacamos su ubicación profunda y alta en la región tóraco-abdominal izquierda y sus complejas relaciones anatómicas derivadas del desarrollo embriológico. Más aún, en caso de patología neoplásica, se suman las controversias con respecto al drenaje linfático extramesocolónico de los tumores que asientan a dicho nivel8 y la relativa baja frecuencia de esta localización.
Clásicamente se describen 3 abordajes para efectuar la movilización completa del AC: anterior, medial y lateral, basándose en la primera maniobra que determina el acceso a la transcavidad de los epiplones.9 No obstante, se trata de una técnica “mixta” o combinada, en la que todos los abordajes son finalmente llevados a cabo, independientemente del orden en que se realicen.
Al margen de ello, la movilización del AE admite variantes en función del tipo de patología a tratar. Concretamente nos referimos a dos escenarios: el primero es la necesidad de efectuar una resección completa del meso y el epiplón mayor en caso de un tumor maligno en esa ubicación;10 el otro es el descenso del ángulo para lograr una anastomosis libre de tensión durante una resección del recto o una restitución del tránsito intestinal.
Siguiendo esta premisa, García-Granero et al.5 describen todas las posibles vías de abordaje en un modelo de disección cadavérica, así como durante el curso de procedimientos quirúrgicos, determinando que existen 5 vías de acceso a la transcavidad de los epiplones (y por lo tanto de abordajes), cuya factibilidad dependerá del escenario planteado (resección vs. descenso). Dicho modelo cadavérico ha sido denominado por los autores como la “caja” del AE (splenic flexure “box”), correspondiendo dicha “caja” a la transcavidad de los epiplones, presentada como propuesta para facilitar y estandarizar la enseñanza de este procedimiento.
Tomando como base este modelo, realizamos una disección cadavérica que nos permitió identificar los ligamentos de fijación, así como efectuar una detallada descripción de la anatomía vascular del ángulo izquierdo y de sus vías de abordaje. Entre éstas pudimos reconocer las siguientes:
Es de gran importancia el conocimiento de la anatomía vascular del AE, particularmente en lo que concierne al abordaje medial, tratándose de un segmento ubicado en la frontera que separa los territorios de la arteria mesentérica superior (AMS) y la AMI. Las conexiones entre ambos son variables y no siempre ha existido consenso acerca de su denominación,14-16 pero se debe estar atento a ellas dado que pueden ser causa de accidentes hemorrágicos durante la sección del mesocolon. Se reconocen las siguientes:
No está claro si la arteria de Moskowitz constituye simplemente una variante anatómica o si se trata de una vía de circulación colateral en circunstancias patológicas, como pueden ser la obstrucción de la AMI o su ligadura previa.18 También se ha investigado la posibilidad de su detección preoperatoria mediante estudios de imagen de alta definición, como la angiotomografía computada 3D, con la consiguiente reducción del riesgo de complicaciones intraoperatorias y además el incremento de la cosecha ganglionar.19
Se justifica plenamente la necesidad de un conocimiento preciso del desarrollo embriológico, la anatomía vascular y las relaciones del AE los ligamentos de fijación y, fundamentalmente, todas las posibles vías de abordaje, sus indicaciones, riesgos y eventuales contraindicaciones.
La movilización del AE es una técnica compleja que requiere sistematización, experiencia y entrenamiento, lo que se traduce en una curva de aprendizaje lenta. Se ha visto que el tiempo que demanda en el curso de una cirugía es de unos 47 minutos en promedio,20 lo que puede aumentar significativamente el tiempo operatorio total en procedimientos como una resección del recto, en los que ha demostrado ser una variable independiente de complicaciones tales como la fuga anastomótica.21
Además, el conocimiento anatómico detallado y correctamente aplicado apunta a alcanzar otros objetivos. Uno de ellos es lograr una técnica quirúrgica de excelencia, que cumpla con los estándares de calidad sobre todo en caso de patología oncológica, como puede ser la realización de una escisión mesocólica completa con ligadura vascular central.22 El otro objetivo se encuadra dentro del concepto de seguridad del paciente, asumiendo que un buen dominio de la técnica y el entrenamiento simulado, son preceptos fundamentales para reducir el índice de complicaciones derivadas de lesiones iatrogénicas, que pueden ocurrir a nivel del bazo, páncreas y uréter fundamentalmente.
El modelo de simulación en cadáver humano ofrece algunas ventajas para la adquisición de estos conocimientos. Tiene una muy buena fidelidad al reproducir exactamente la anatomía humana y, permite diseñar estrategias de enseñanza y entrenamiento (splenic flexure “box”) bastante atractivas y reproducibles, como hemos podido demostrar en nuestra experiencia.
Sin embargo, el modelo cadavérico también presenta ciertas limitaciones. Para empezar, su disponibilidad es variable y muchas veces sujeta a restricciones éticas y legales. Además, no ofrece la posibilidad de reutilización y, por lo tanto, su aplicabilidad está restringida a una sesión de entrenamiento puntual más que a la práctica de tipo distributiva o continuada, en la que se puede observar progresión a lo largo del tiempo.23,24
Por otra parte, la rigidez y poca complacencia de los tejidos cadavéricos sometidos a fijación (incluso en el cadáver fresco) dificultan su uso para la simulación de procedimientos laparoscópicos. Una alternativa es la conservación con el método descrito por Walter Thiel,25 en el que la inmersión en una solución específica permite conservar las propiedades físicas de los tejidos y por lo tanto los hace más apropiados para entrenar procedimientos invasivos.
En nuestro país, con una población pequeña y centros que suelen ser de bajo volumen, es imperativo que los cirujanos conozcan este tipo de herramientas, si ello logra hacer más efectivo el aprendizaje de procedimientos quirúrgicos de alta complejidad. Se trata de un modelo de simulación y enseñanza ya validado,5 y que hemos logrado reproducir, demostrando su aplicación y buena correlación con el escenario real.
CONCLUSIONES
El modelo cadavérico permite efectuar un estudio detallado de la anatomía vascular del AE, sus medios de fijación y sus relaciones, y simular las vías de abordaje para su movilización completa. Estos conocimientos facilitan el abordaje quirúrgico, cuya realización por vía laparoscópica sigue siendo un desafío técnico.
Agradecimientos
Al Departamento de Anatomía de la Facultad de Medicina (Universidad de la República), por su colaboración aportando el material cadavérico utilizado.
REFERENCIAS