Traumatismos de Colon.
Diagnóstico y Tratamiento de Lesiones Penetrantes
y No Penetrantes
Pablo Ezequiel Finno
Residente de cuarto año de clínica quirúrgica del Hospital Interzonal General de Agudos
Luisa Cravenna de Gandulfo. Lomas de Zamora, Buenos Aires.
Año 2016
Esta monografía es propiedad de la Sociedad Argentina de Coloproctología y no puede ser publicada, en todo o en parte, o resumirse, sin consentimiento escrito de la Comisión Directiva de esta Sociedad y de su autor.
INTRODUCCIÓN
Realizo esta monografía a fin de cumplir con los requisitos de aprobación del “35° Curso Anual de Coloproctología 2016” organizado por la Sociedad Argentina de Coloproctología. El tema que voy a desarrollar es traumatismos de colon. Para ello realizaré una búsqueda bibliográfica en castellano e inglés presentando el diagnostico y tratamiento de las lesiones penetrantes y no penetrantes del colon.
HISTORIA
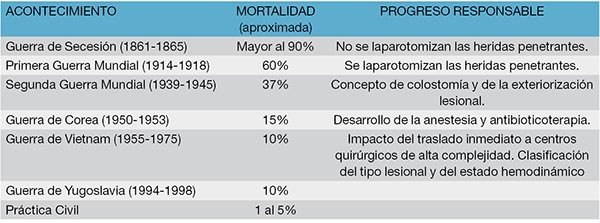
La experiencia obtenida por los cirujanos militares en las lesiones del colon producidas durante los diferentes acontecimientos bélicos durante el último siglo, han logrado generar avances en cuanto a su manejo y tratamiento.
Durante la Guerra de Secesión, que tuvo lugar en estados unidos entre los años 1861 y 1865, la mortalidad de las heridas del colon era entre el 90 y el 100%.1,2
En el año 1916, durante la primera Guerra Mundial, el cirujano inglés Wallace hizo la primera descripción detallada del manejo de las lesiones del colon producidas por heridas de arma de fuego. El 66% de las mismas fueron tratadas mediante reparación primaria con una mortalidad del 50%, mientras que en el 34% se les realizó colostomía con una mortalidad del 73,5%.3 Se llegó a la conclusión que las heridas colónicas podían tratarse en forma segura mediante la sutura primaria considerando las colostomías proximales beneficiosas en lesiones extensas y las ubicadas en el colon izquierdo. En el año 1917, Fraser, cirujano militar inglés, reportó el primer caso de sepsis retroperitoneal secundario a una herida colónica.3
En octubre de 1943, el Servicio de Cirugía General de las Fuerzas Armadas de los EEUU decidió (basándose en los reportes recogidos por Ogilvie durante la Campaña del Desierto del Norte de África) que la totalidad de las heridas colónicas producidas durante la Segunda Guerra Mundial debían ser tratadas mediante colostomía. De esta forma se logró una disminución de la mortalidad al 30%.3 Durante la Guerra de Corea y de Vietnam se logró un descenso de la mortalidad de las heridas colónicas al 10–15%, mientras que en los conflictos de Croacia-Bosnia (Guerra de Yugoslavia), la mortalidad global fue del 10,1%.4
Se quisieron trasladar todos los conocimientos adquiridos para el manejo de las heridas colónicas durante los conflictos bélicos a la vida civil pero las características de los agentes traumáticos eran distintas. Fue así que durante la década de los 50 diferentes centros sugirieron la resolución de las heridas colónicas mediante la reparación primaria. En 1951, Woodhall y Ochsner reportaron una mortalidad del 9% en los pacientes tratados con reparación primaria y de un 40% en aquellos tratados con colostomía. En 1961, Isaacson reportó una mortalidad del 2,05% para los pacientes con reparación primaria y un 17% para los pacientes a los que se les realizó colostomía. A fines del año 1980, la reparación primaria había reemplazado a uso de la colostomía en el tratamiento de las mayoría de los civiles con lesiones colónicas en los centros de trauma urbano.3
Con la mejora de los sistemas de traslado, de las maniobras de reanimación, uso de antibióticos y transfusiones sanguíneas y la rápida intervención quirúrgica se logró un descenso de la mortalidad de las heridas colónicas a cifras que oscilan entre el 1 al 5% (Tabla 1).5,6
Tabla 1: Evolución de la mortalidad en los traumatismos colónicos
ANATOMÍA QUIRÚRGICA DEL COLON
El colon o intestino grueso se extiende desde el yeyunoíleon hasta el ano. Tiene una longitud aproximada de 1,50 metros, formando un marco alrededor del intestino delgado. Se diferencia de este por su mayor calibre, por presentar 3 cintillas longitudinales (bandeletas o tenias) que convergen en la base de implantación del apéndice cecal y por presentar apéndices epiplóiocos y haustras.7
Desde la anatomía descriptiva se lo divide en las siguientes porciones: ciego, apéndice cecal, colon ascendente, colon transverso, colon descendente, colon sigmoideo y recto (fig. 1).8
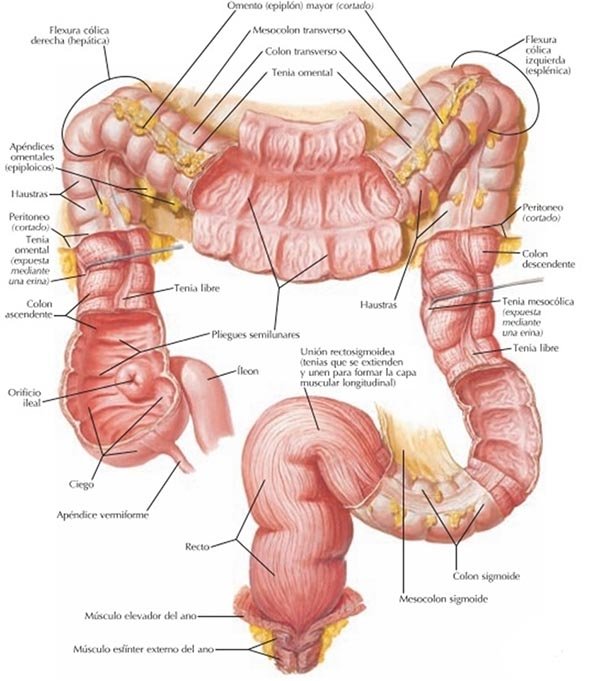
Figura 1: Anatomía descriptiva del colon.
Desde la anatomía quirúrgica se divide al colon en los siguientes sectores:
- Colon derecho: Desde al ángulo ileocecal hasta que el colon transverso cruza la segunda porción del duodeno. Incluye: cecocapendice, colon ascendente, ángulo hepático y la porción del colon transverso que llega hasta el límite determinado.
- Colon Izquierdo: Desde el borde izquierdo del colon transverso que atraviesa la segunda porción del duodeno hasta la cresta ilíaca izquierda. Incluye: resto del colon transverso, ángulo esplénico y colon descendente.
- Colon Pelviano: Desde la cresta ilíaca izquierda hasta la tercera vértebra sacra. Incluye: colon sigmoideo.
- Recto: Desde la tercera vértebra sacra hasta el anillo anorectal. Se continúa con el conducto anal que se extiende desde el anillo anorectal hasta el margen cutáneo mucoso del ano.
El intestino grueso está constituido, por cuatro túnicas superpuestas que son: serosa, muscular, submucosa y mucosa.
El ciego tiene la forma de un saco abierto hacia arriba. Mide cerca de 6 cm. de alto y de 6 a 8 cm. de ancho. Está normalmente situado en la fosa ilíaca derecha. Su dirección es oblicua hacia abajo, hacia adentro y hacia adelante. Presenta: cuarto caras (anterior, posterior, externa e interna), una extremidad superior o base por la cual el ciego se continúa con el colon ascendente, y una extremidad inferior o fondo, que es libre y redondeada. Por arriba de la cara interna está el orificio de desembocadura del intestino delgado. La porción terminal del yeyunoíleon forma con el ciego un ángulo agudo abierto hacia abajo y a la izquierdo, el ángulo ileocecal. Sus relaciones son: cara anterior con el peritoneo parietal anterior y asas intestinales, cara posterior con el peritoneo parietal posterior, cara lateral con el peritoneo parietal lateral y cara medial con los vasos ilíacos, asas intestinales y el apéndice cecal.
El apéndice cecal constituye un divertículo alargado de 7,5 a 10 cm. de longitud y de un diámetro de 0,6 cm. Nace en la cara posterointerna del ciego, a 2,5 cm de la válvula ileocecal en la convergencia de las tres bandeletas longitudinales (anterior, posteroexterna y posterointerna) del ciego. En el 65% de los pacientes se ubica detrás del ciego, en el 30% se encuentra en dirección a la pelvis, y en el resto se presenta por debajo del ciego, o por delante y por detrás del íleon.
El colon ascendente mide entre 8 y 15 cm. de longitud de dirección hacia arriba y atrás hasta la formación del ángulo hepático. Hacia posterior, a través de su Fascia de coalescencia Told II o derecha se relaciona con la cara anterior del riñón derecho y el uréter, con el cuadrado de los lomos y la aponeurosis del músculo transverso por arriba, y por abajo, con el músculo ilíaco, la cresta ilíaca y el ligamento ileolumbar.
El ángulo hepático del colon suele ser agudo. Está orientado en un plano vertical oblicuo y su abertura mira hacia adentro, abajo y adelante. Se relaciona con la cara inferior del hígado, la vesícula biliar, el pedículo hepático, el píloro y la porción supramesocólica del duodeno. El ángulo cólico derecho está suspendido y fijo por un sistema de ligamentos que son generalmente avasculares y que se disponen en tres planos:
A. Superficial: epiplocoloparietal;
B. Medio: hepatocólico, cistocólico y duodenocólico;
C. Profundo: renocólico y frenocólico.
El colon transverso tiene una longitud que varia entre 40 y 80 cm. (con un promedio de 50 cm.). Se pueden distinguir dos partes, cuyo límite está sobre el borde interno de la segunda porción del duodeno. La parte derecha es fija y se dirige hacia delante, abajo y adentro; la parte izquierda es más larga y móvil y esta unida a la pared por el mesocolon transverso; se dirige hacia la izquierda, atrás y arriba. El colon transverso es un asa cóncava hacia arriba y atrás, y su extremidad izquierda esta más alta que la derecha. Se relaciona hacia adelante con el hígado en su extremo derecho y en todo el resto con la pared abdominal anterior por intermedio del epiplón mayor. Hacia arriba el segmento fijo esta en contacto con el hígado, su segmento móvil bordea la curvatura mayor del estomago hasta el bazo. Hacia atrás se aplica, de derecha a izquierda, sobre el riñón derecho, la segunda porción del duodeno, cabeza del páncreas, tercera porción del duodeno, asas de delgado y riñón izquierdo. Hacia abajo contacta con las asas de intestino delgado.
El ángulo esplénico del colon es más agudo que el ángulo hepático. Su abertura mira hacia delante, abajo y adentro. Se relaciona con la parte media del riñón izquierdo, la curvatura mayor del estomago, el bazo, la pared abdominal y el diafragma. Sus puntos de fijación se disponen en tres planos: el superficial o ligamento frenocólico izquierdo, el medio constituido por el ligamento de Buy y el esplenomesocólico y el profundo formado por el ligamento parietocólico.
El colon descendente se extiende desde el ángulo izquierdo hasta el inicio del colon pelviano. Desciende en dirección vertical y tiene una longitud media de 12 cm. Está fijo a la pared posterior por la Fascia de coalescencia de Told III o izquierda. Su cara posterior está en relación con el borde externo del riñón izquierdo y la pared abdominal (cuadrado lumbar) y sus caras anterior y lateral contactan con las asas intestinales.
El colon sigmoide mide aproximadamente 40 cm. de longitud y continúa al colon descendente. Comienza a nivel del borde interno del músculo psoas izquierdo y termina en el recto a nivel de la tercera vértebra sacra. Es móvil, se encuentra suspendido a la pared por un mesocolon extenso, siendo su situación, relaciones y movilidad variables.
El ciego, apéndice cecal, colon ascendente, ángulo hepático y mitad proximal del colon transverso, están irrigados por las ramas colaterales derechas que se desprenden de la arteria mesentérica superior. Ésta nace a nivel de la cara anterior de la aorta a la altura de la doceava vértebra dorsal o primera lumbar. Las ramas que irrigan al colon derecho son la cólica superior derecha, la cólica media y la cólica inferior o ileobicecoapendiculocólica. Éstas arterias cuando se dirigen hacia el colon se bifurcan como una “T” uniendo sus respectivos ramos, las que ascienden con las que descienden, a dos centímetros del borde mesentérico del colon y constituyen a manera de arcada la arteria marginal de Sudeck. De ella se desprenden los vasos rectos. La rama marginal ascendente que se forma a partir de la cólica superior y que se encuentra ubicada en el espesor derecho del mesocolon transverso, se anastomosa con la rama marginal descendente que proviene de la cólica superior izquierda, colateral de la arteria mesentérica inferior, para constituir la arcada marginal de Riolano que nutre el colon transverso (fig. 2).8
El colon izquierdo y la porción superior del recto están irrigados por la arteria mesentérica inferior. Ésta emerge de la pared anterolateral izquierda de la aorta abdominal a la altura de la tercer o cuarta vértebra lumbar, a 4 cm. por encima de la bifurcación aórtica y a 2 cm. por encima del promontorio. Sus colaterales principales son la arteria cólica superior izquierda y el tronco de las sigmoideas. La rama terminal de la arteria mesentérica inferior es la arteria hemorroidal superior. Es la encargada de irrigar a la porción superior del recto. La arteria hemorroidal media, rama de la arteria hipogástrica y la arteria hemorroidal inferior, rama de la arteria pudenda interna, son las encargadas de irrigar al recto medio e inferior respectivamente.
El drenaje venoso se realiza acompañando las arterias respectivas. La vena mesentérica superior discurre a la derecha de su arteria homónima para terminar anastomosándose por detrás del páncreas para constituir el origen de la vena porta con el tronco esplenomesaraico, la gastroepiploica derecha, la coronario estomaquica y la pilórica. En un 60% de los casos, las tres últimas ramas se unen en un tronco común (Tronco de Henle) que desemboca en la vena mesentérica superior cerca del origen de la vena porta.
La vena mesentérica inferior resume la circulación procedente de las venas cólicas izquierdas y las sigmoideas. Se ubican a la izquierda de su arteria homónima, la que excede por arriba unos 5 a 8 cm. de su origen, para desembocar detrás del páncreas en la vena esplénica, y formar el tronco esplenomesaraico. La circulación venosa del conducto anal por encima de la línea pectínea es a través de la vena dorsal del recto, la cual desemboca en la vena mesentérica inferior y es parte integrante del sistema porta. A su vez a través de la anastomosis del plexo hemorroidal superior con los plexos hemorroidales medios e inferiores constituyen un sistema de derivación portocava utilizando las venas ilíacas internas y pudendas internas.
El drenaje linfático del colon se efectúa por dos vías que se intercomunican, a) el plexo linfático intramural que conforman una red submucosa y subserosa y b) linfáticos extramurales constituidos por vasos y ganglios que acompañan los vasos cólicos.
La inervación del colon procede de los plexos mesentéricos superior e inferior. El recto está inervado por los plexos hemorroidales superiores (que son la terminación del plexo mesentérico inferior), por los plexos hemorroidales (que emanan de los plexos hipogástricos) y por el nervio hemorroidal o anal (rama del plexo sacro).
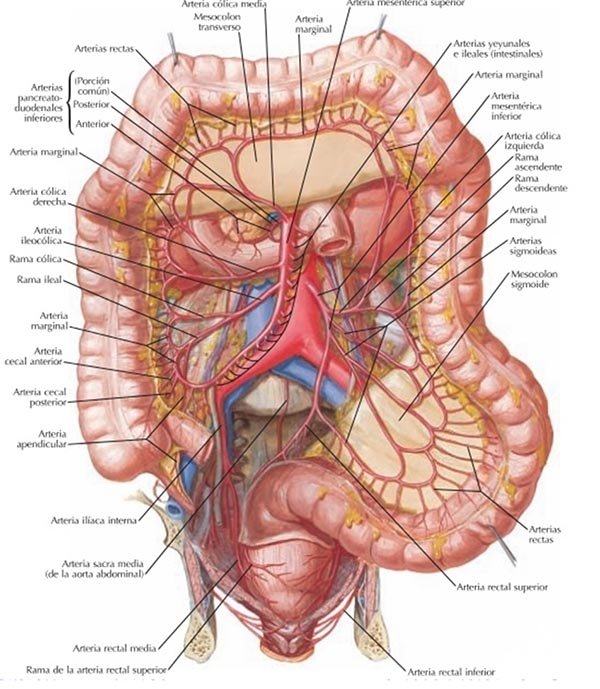
Figura 2: Irrigación del colon.
FRECUENCIA
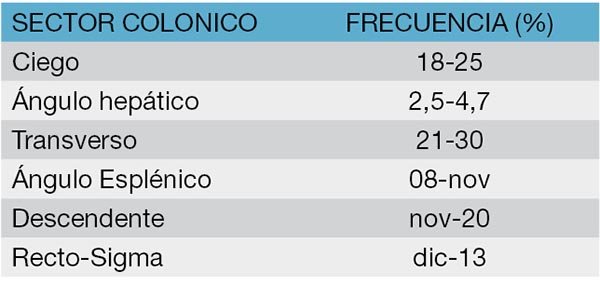
La frecuencia de las lesiones colónicas producto de los traumatismos de abdomen es variable. En la tabla 2 se observa su incidencia según las distintas series publicadas.
En la tabla 3 se expone la distribución topográfica de las lesiones traumáticas del colon.13
Tabla 2: Frecuencia de las lesiones colónicas en los traumatismos de abdomen

Tabla 3: Distribución topográfica de las lesiones en el colon
ETIOLOGÍA
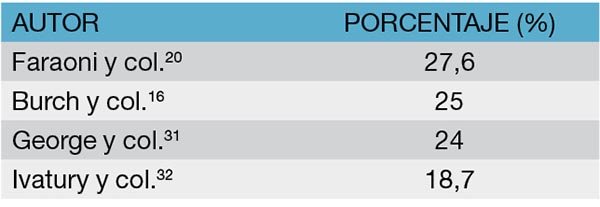
De acuerdo con Dezanzo y col.14 los traumatismos de colon pueden ser clasificados en dos grupos (graf. 1):
A. Traumatismos de colon por agentes no penetrantes.
B. Traumatismos de colon por agentes penetrantes.
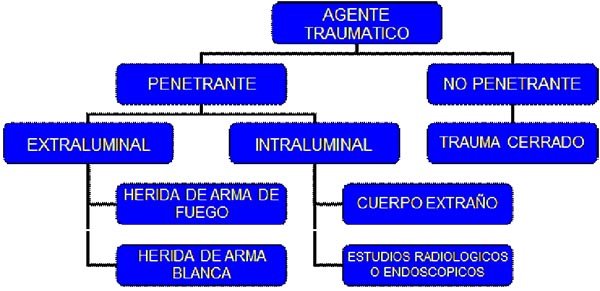
Gráfico 1: Modalidad traumática de las lesiones colónicas.
Los caracterizaré a continuación:
Traumatismos por agentes no penetrantes
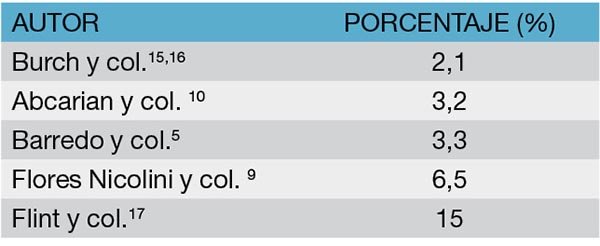
Estas lesiones aparecen como consecuencia de traumatismos cerrados de abdomen. La frecuencia de aparición varía entre el 2,1% y el 15% (Tabla 4). En las zonas rurales la incidencia de lesiones colónicas por traumatismos no penetrantes es mayor.
Los accidentes automovilísticos constituyen su causa principal; en menor medida, se deben a los accidentes laborales y de tránsito. En un trabajo multicéntrico, Muche y col.3 hallaron sobre 361 lesiones colónicas por agentes romos que el 72% se debían a accidentes automovilísticos, el 10% por accidentes de tránsito, el 8% por accidentes de moto y en el 6% por accidentes de trabajo.
Las lesiones colónicas provocadas por agentes no penetrantes son contusas, en general extendidas, anfractuosas, de bordes desflecados, con destrucción tisular, sin límites netos y con compromiso de la irrigación colónica por desprendimiento o desgarro de su meso.
Tabla 4: Frecuencia de las lesiones colónicas en los traumatismos no penetrantes de abdomen
En las contusiones, el daño intestinal puede ser ocasionado por tres mecanismos:
A. Directo: debido al aplastamiento del intestino sobre el plano rígido osteomuscular.
B. Por desgarro: en las zonas fijas del colon (ángulo hepático y/o esplénico).
C. Por aumento de la presión endoluminal y formación de un asa cerrada al comprimirse simultáneamente los dos pies de ésta.
En la serie de State y col.17 en los traumatismos por agentes romos, el colon transverso fue el más frecuentemente lesionado (39%), seguido por el cecoascendente (29%), el colon izquierdo (21%) y el recto intraperitoneal (11%). Las lesiones de mayor gravedad se hallaron en el cecoascendente y en el colon izquierdo.
Traumatismos por agentes penetrantes
Constituyen la causa más frecuente de lesiones colónicas. Su frecuencia según las distintas series figura en la tabla 5.
Las lesiones penetrantes pueden ser originadas por agentes intraluminales o extraluminales.
Los agentes intraluminales lesionan el colon desde el interior de la luz hacia el peritoneo y corresponden a:
A. Cuerpos extraños ingeridos (huesos de pollo, escarbadientes, espinas de pescado, prótesis dentaria, etc.).
B. Cuerpos extraños introducidos por vía anal:
C. I. Empalamientos o con fines masturbatorios.
II. Iatrogénicos: estudios endoscópicos y/o contrastados.
La ingestión accidental de cuerpos extraños ocurre generalmente en niños y ancianos. En el 90% de los casos pasan a través de todo el tracto digestivo y no requieren tratamiento, mientras que el 1% requiere de extracción quirúrgica.21 Algunos se enclavan a distintas alturas del colon provocando cuadros perforativos, fistulosos o tumorales inflamatorios. Los que tienen una longitud mayor de 6 cm. quedan retenidos en el estómago y los de menor longitud se pueden impactar en la válvula ileocecal ocasionando cuadros suboclusivos. De los cuerpos extraños ingeridos voluntariamente, entre el 10 y el 20% deben ser extraídos endoscópicamente y entre el 1 y el 14% requieren de extracción quirúrgica. En la serie de Velitckov y col.22 el 75,6% de los cuerpos extraños ingeridos fueron eliminados por vía natural. En el 19,5% se recurrió a la extracción endoscópica y el 4,8% requirió cirugía para su remoción.
Tabla 5: Frecuencia de las lesiones colónicas en los traumatismos penetrantes de abdomen
Las lesiones por cuerpos extraños introducidos por el ano se deben generalmente a prácticas homosexuales, autoerotismo o a fenómenos de ultraje. La mayoría de las lesiones producidas involucran al recto (lesiones esfinterianas) y en menor medida a la unión rectosigmoidea o el sigma. Los elementos utilizados son vibradores, falos de goma, envases de desodorantes, vegetales como zanahoria, choclos, etc. Estos agentes traumáticos provocan lesiones perforativas de bordes netos o desflecados, con tejido necrótico por impactación. En general, este tipo de lesiones son ocultadas por algún tiempo, lo que favorece a que se expresen mediante cuadros peritoneales asociados a celulitis perianales.
Las lesiones del colon pueden ser generadas por estudios endoscópicos. La incidencia de perforación colónica debido a la rectosigmoideoscopía (ubicada en la cara anterior del ángulo rectosigmoideo) oscila entre 0,018 y 0,025%.23 En la colonoscopía diagnóstica, la frecuencia es del 0,1 al 0,8% y para las terapéuticas oscila entre el 0,5 y el 3%.24,25,26,27,28 El mecanismo de producción puede ser mecánico, por presión neumática o por la toma de biopsias, coagulación o polipectomía generando cuadros peritoneales localizados o difusos.
Otro tipo de lesión iatrogénica colónica corresponde a la que se ocasiona durante estudios contrastados tales como el colon por enema con bario. Según las distintas series, su incidencia oscila entre el 0,016 y el 0,4%.29 Los mecanismos de producción involucrados son: traumatismo de la cánula de enema, distensión excesiva del balón rectal o barotrauma debido a la gran presión por la distensión. La presencia de una patología colónica predispone a este tipo de perforación; por ejemplo: la enfermedad diverticular, las neoplasias o la enfermedad inflamatoria intestinal. Otros factores son la edad avanzada, el uso de corticoides y las biopsias realizadas en días anteriores al estudio contrastado.
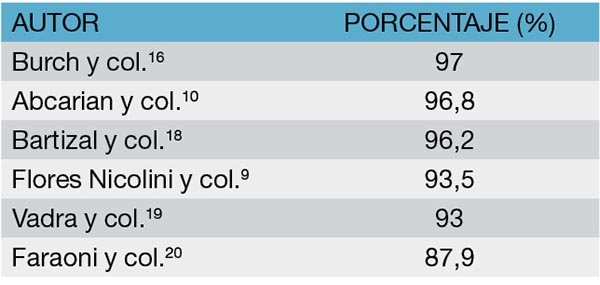
Los agentes extraluminales lesionan al colon desde el exterior hacia la luz del órgano y están constituidos por las heridas de arma de fuego y las heridas de arma blanca. Son la causa más frecuente de lesiones del colon (90 al 97%), predominando en pacientes de sexo masculino entre la segunda y quinta década de la vida.
Las heridas de arma de fuego son, dentro de las lesiones penetrantes del colon, las de mayor frecuencia. Su incidencia oscila entre el 68 y el 76% (Tabla 6). Si bien se comporta como un elemento perforante, la capacidad lesiva del proyectil depende de la energía cinética liberada en los tejidos. Torino y col.11 expone una frecuencia de lesiones asociadas del 71,1% y Garcia y col.12 del 91,4%. Según Barwich y col.30 el órgano más frecuentemente asociado a la lesión colónica es el intestino delgado (Tabla 7).13 Es necesario tener en cuenta que la perforación generada está condicionada, además, por un halo de necrosis circundante, que puede llegar hasta 2 cm más allá de la lesión propiamente dicha.
Las lesiones del colon ocasionadas por heridas de arma blanca tienen una frecuencia de alrededor del 18 al 25% (Tabla 8). Generalmente son lesiones lineales, de bordes netos, con escaso daño tisular y mínimo compromiso vascular. Es excepcional que se lesione más de una cara del colon.
Tabla 6: Frecuencia de las lesiones colónicas por herida de arma de fuego
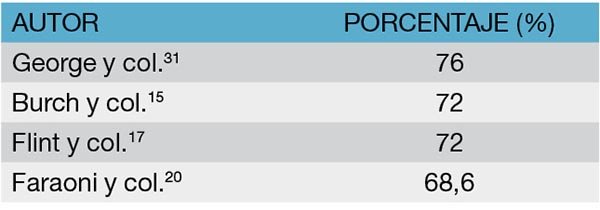
Tabla 7: Frecuencia de las lesiones asociadas en los traumatismos penetrantes del colon
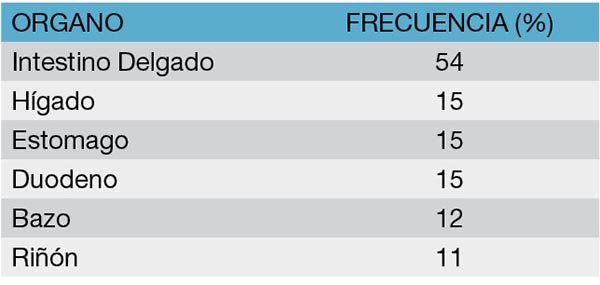
Tabla 8: Frecuencia de las lesiones colónicas por herida de arma blanca
MANIFESTACIONES CLÍNICAS
Tanto en los traumatismos cerrados como en los abiertos las manifestaciones clínicas son inespecífica. Se puede presentar como un abdomen agudo perforativo o hemorrágico en relación con el tipo de lesión colónica y al de las lesiones asociadas. George y col.31, 33 enfatizan sobre la importancia de los primeros signos físicos en el examen abdominal.
En los traumatismos cerrados, la manifestación clínica más importante es el dolor abdominal espontáneo. Éste se incrementa con la palpación, apareciendo defensa muscular y reacción peritoneal, en ausencia de ruidos hidroaéreos. En los primeros momentos post traumatismo el cuadro clínico puede ser más solapado. La proctorragia es un signo importante de lesión ano-rectal. El shock, si está presente, empeora el pronóstico. En pacientes con alteración del sensorio, por traumatismo de cráneo, alcoholizados o bajo los efectos de drogas de abuso, el examen abdominal puede no dar datos útiles, requiriéndose de estudios complementarios para arribar al diagnóstico. Ross y col.34 expusieron que solo el 5% de las lesiones colónicas por traumatismos romos eran diagnosticadas en el preoperatorio; la mayoría de las mismas fueron descubiertas en el momento de la laparotomía exploradora indicada por otros motivos.
En los traumatismos penetrantes, el cuadro clínico es similar al de los traumatismos cerrados; ocasionalmente se agrega la evisceración. En las heridas de arma blanca, si el paciente esta estable hemodinamicamente, es factible la exploración local de la herida para determinar la penetración a la cavidad abdominal. En las heridas de arma de fuego, si bien hay algunas excepciones, es mandatario la exploración quirúrgica. El diagnóstico de lesión colónica es realizado normalmente durante la lapatoromía. En las lesiones endoluminales por estudios endoscópicos, el dolor abdominal intenso y brusco asociado a la visualización directa de la perforación son determinantes. En la perforación por enclavamiento de espinas de pescado o fragmentos de huesos de pollo, el dolor y los signos de irritación peritoneal son progresivos. La lesión ano-recto-colónica por introducción de objetos por el ano se puede sospechar por proctorragia y dolor abdominal o anal (fisuras).
El tacto rectal es muy útil en todo paciente politraumatizado, ya que se puede determinar la presencia de sangre, palpar una perforación rectal, fragmentos óseos o elementos extraños endoluminales, evaluar el tono esfinteriano (lesión medular), determinar la posición prostática (lesión de uretra posterior) y detectar hematomas que comprimen el recto o crepitación perirrectal.35
ESTUDIOS COMPLEMENTARIOS
La intervención quirúrgica de urgencia está indicada en todo paciente con inestabilidad hemodinámica, proctorragia o en presencia de signos peritoneales. Ante duda diagnóstica se procederá a realizar los siguientes estudios complementarios:
A. Laboratorio: Aporta datos relativos a la situación clínica y hemodinámica del paciente. Orienta hacia el tipo de lesión asociada.
B. Radiografía simple de abdomen: Puede mostrar neumoperitoneo, aire en el retroperitoneo en el 60 al 65% de los casos o pérdida de la sombra de los psoas. Estos hallazgos son indicación de exploración quirúrgica. La presencia de íleos regionales hace sospechar lesiones mínimas bloqueadas o abscedadas. Permite realizar el seguimiento de la progresión de los cuerpos extraños ingeridos, y localizar aquellos que son introducidos por el ano, cuando son radiopacos.13, 35
C. Ecografía abdominal: Tiene una alta sensibilidad para el diagnóstico de líquido libre en cavidad (90%) pero baja (entre el 34,7 y el 48%) para el diagnóstico de lesión de víscera hueca.13, 35
Lavado peritoneal diagnóstico: Es positivo y específico para lesión intestinal si presenta fibras de alimentos, bacterias o bilis. Al igual que ante la presencia de sangre, la laparotomía es la regla. Presenta del 2 al 7% de falsos negativos.13, 35
D. Tomografía axial computada (TAC): Requiere de estabilidad hemodinámica para su realización. Detecta lesiones asociadas, principalmente de órganos sólidos (hígado, riñón y bazo) y de estructuras óseas. Orienta hacia el diagnóstico de lesión intestinal si muestra: aire, líquido intraperitoneal que no esté cerca de un órgano sólido lesionado, engrosamiento de la pared intestinal o hematoma en el mesocolon con una sensibilidad del 97%. Estos hallazgos justifican la laparotomía.13, 35
E. Laparoscopía: Detecta con exactitud la penetración peritoneal. Es útil para el diagnóstico de lesiones diafragmáticas, de órganos sólidos y de hemoperitoneo, no así para revelar lesiones colónicas o de otras vísceras huecas.
F. Anoscopía, Rectosigmoideoscopía (RSC) y Colonoscopía (CC): De utilidad para el diagnóstico de fisuras anales, perforaciones y lesiones recto-colónicas sangrantes, y para detectar fragmentos óseos o cuerpos extraños endoluminales.
A continuación se expondrá en los gráficos 2, 3, 4 y 5 los algoritmos de diagnóstico y manejo de las lesiones colónicas en los traumatismos abiertos y los traumatismos cerrados.35
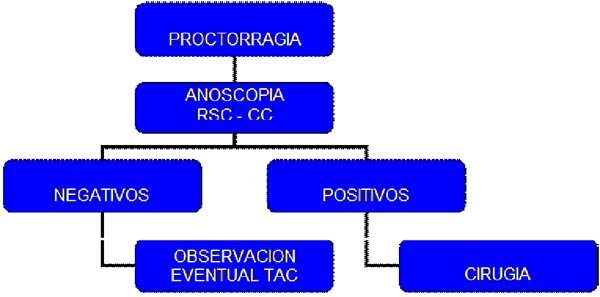
Gráfico 3: Algoritmo diagnóstico y manejo de las lesiones colónicas en pacientes con proctorragia por traumatismo cerrado de abdomen y pelvis.

Gráfico 4: Algoritmo diagnóstico y manejo de las lesiones colónicas en pacientes con inestabilidad hemodinámica o signos peritoneales por traumatismo cerrado de abdomen y pelvis.
CLASIFICACIÓN
Existe una diversidad de formas de clasificar a las lesiones colónicas, entre ellas:
Penetrating Abdominal Trauma Index (PATI)
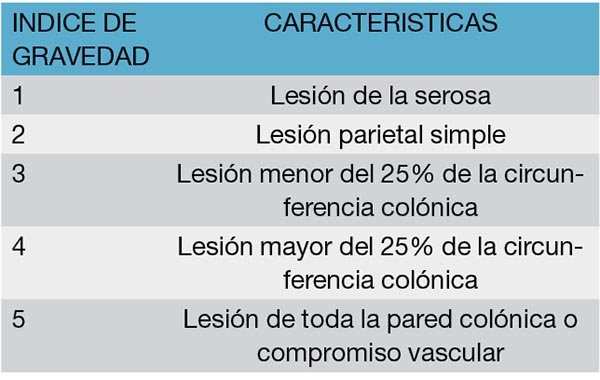
El PATI es el índice más detallado para predecir la evolución del traumatismo, aunque no considera el impacto fisiológico de las lesiones de otras partes del cuerpo. Se basa en la combinación de la severidad de las lesiones individuales de cada víscera diagnosticadas intraoperatoriamente. A la lesión de cada órgano se le asigna un número de 1 a 5 de acuerdo a su gravedad. El resultado del PATI surge de multiplicar el número correspondiente a la gravedad de la lesión por el coeficiente de riesgo de cada órgano. Al colon se le adjudica el factor de riesgo 4 y se establecen cinco categorías de gravedad (Tabla 9).36
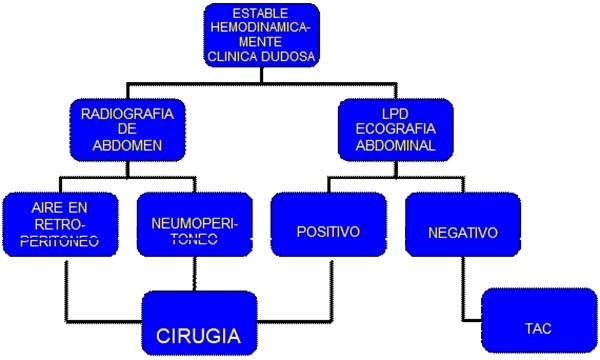
Gráfico 5: Algoritmo diagnóstico y manejo de las lesiones colónicas en pacientes con estabilidad hemodinámica o clínica dudosa por traumatismo cerrado de abdomen y pelvis.
Tabla 9: Penetrating Abdominal Trauma Index (PATI)
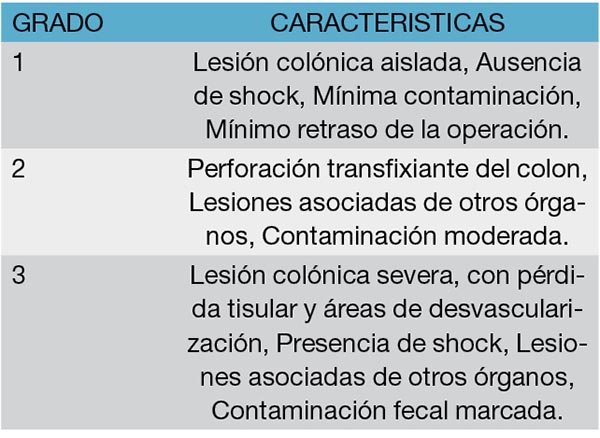
Flint Colon Injury Score
Las heridas colónicas están divididas en tres grupos de gravedad creciente (Tabla 10).17
Tabla 10: Flint Colon Injury Score
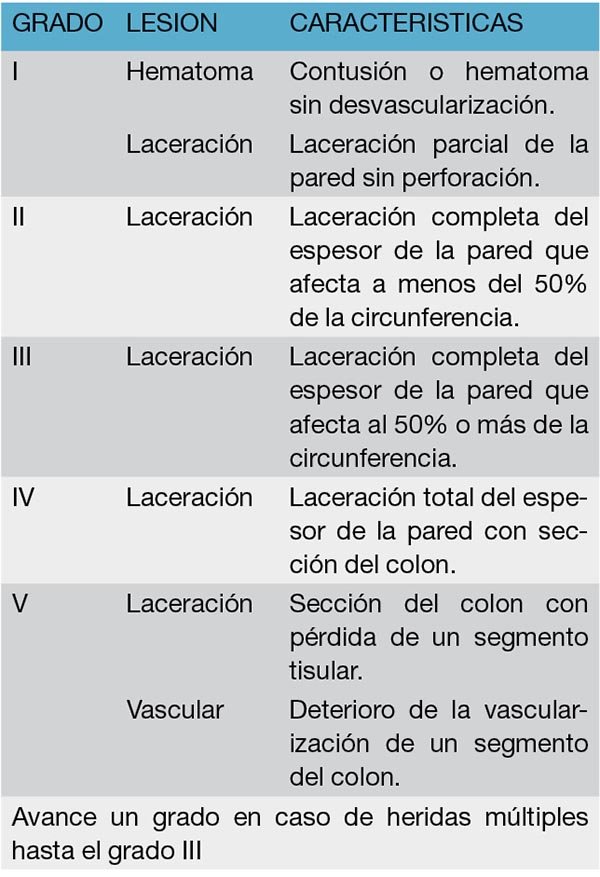
Colon Injury Scale (CIS) / Colon Organ Injury Scale (COIS)
The American Association for the Surgery of Trauma (AAST) elaboró la Colon Injury Scale (Tabla 11) para describir las diversas lesiones traumáticas del colon.37
La AAST, a través del comité de estadificación de lesiones orgánicas, ha modificado la clasificación inicial estableciendo la Colon Organ Injury Scale (Tabla 12).37
Las lesiones no destructivas del colon corresponden a un FLINT 1 y 2 y a un COIS I, II, y III. Las lesiones destructivas del colon corresponden a un FLINT 3 y a un COIS IV y V.
Tabla 11: Colon Organ Injury Scale (CIS)

Tabla 12: Colon Organ Injury Scale (COIS)
FACTORES DE RIESGO
Los factores de riesgo que influyen en la morbimortalidad de las lesiones traumáticas del colon son:
Shock
La hipotensión sostenida (Tensión arterial sistóloca -TAS- < 90 mmHg) en el pre o intraoperatorio aumenta significativamente la morbimortalidad.31 Burch y col.16 reportaron una mortalidad del 5,6% en los pacientes que tuvieron hipotensión previa a la cirugía, mientras que fue del 26,7% en aquellos con hipotensión intraoperatoria y del 58% si el shock persistió antes y durante la intervención quirúrgica.
Contaminación fecal
George y col.33 clasificaron la contaminación fecal como escasa, si el derrame se hallaba confinado al área inmediata a la zona de la herida, moderada, si el derrame comprometia un cuadrante del abdomen y masiva, si el volumen de materia fecal comprometía más de un cuadrante del abdomen. Tanto en las series de Flores Nicolini y col.9 como de Ross y col.34 se llegó a la conclusión que este es el factor de mayor riesgo en la infección postoperatoria. Nelken y col.38 tuvieron un índice de complicaciones del 19,6% en pacientes con contaminación fecal mínima, mientras que fue del 63% en pacientes con contaminación fecal moderada a severa.
Transfusión sanguinea
George y col.31 hallaron un índice de 30% de complicaciones sépticas en pacientes que recibieron menos de cuatro unidades de glóbulos rojos, en comparación con el 69% de aquellos que recibieron más de cuatro unidades. Nelken y col.38 reportaron un índice de complicaciones del 13,5% y del 81% respectivamente.
Tiempo de evolución
El retraso en el tratamiento de las lesiones colónicas incrementa la contaminación fecal y la perdida sanguínea intraperitoneal, ambos factores agravantes en el desarrollo de complicaciones infecciosas.39 El tiempo ideal límite para la reparación primaria es de entre 6 y 8 horas de producida la lesión.
Agente traumático y lesiones asociadas
Según Thompson y col.40 el 75% de las lesiones colónicas se hallan asociadas a lesiones en otros órganos (Tabla 13).
Las heridas de arma de fuego tienden a provocar lesiones severas del colon asociadas generalmente a lesiones de otros órganos lo que aumenta significativamente la morbimortalidad (Tabla 14).13, 39
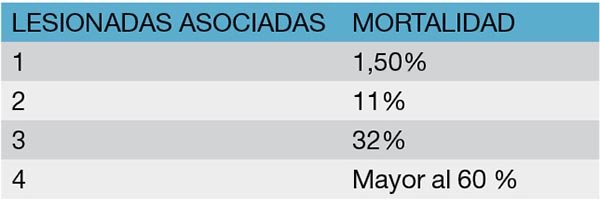
Burch y col.15,16 hallaron una relación directa entre el número de lesiones asociadas y la mortalidad.
Vadra y col.19 citan una mortalidad de 3,22% cuando la lesión colónica fue única, mientras que esta cifra ascendió al 10,71% cuando los órganos lesionado serán dos y al 66% cuando eran cuatro o más.
Las heridas de arma blanca producen lesiones menos severas, más aptas para la reparación primaria. Los traumatismos por agentes romos generan lesiones con grave compromiso de la pared colónica, con afección de sus mesos lo que condiciona un riesgo mayor de complicaciones.
Según Nelken y col.38 un PATI menor a 25, un CIS menor de 25 y un Flint menor o igual a II, son indicadores favorables para la realización de una reparación primaria.
Tabla 13: Números de órganos lesionados asociados a los traumatismos de colon
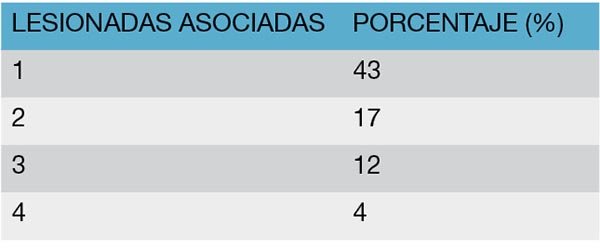
Tabla 14: Mortalidad según lesión asociada
Edad
Burch y col.15, 16 hallaron una significativa diferencia en la mortalidad de los pacientes mayores de 40 años (20,7%) en relación a los más jóvenes (7,4%).
TRATAMIENTO
Atención inicial
El manejo inicial de todo paciente politraumatizado se hará en base a los protocolos de atención del ATLS (Advanced Trauma Life Support) propuestos por el Colegio Americano de Cirujanos (ACS, por sus siglas en ingles) el cual consiste de una revisión primaria rápida, de una reanimación y restauración de sus funciones vitales, de una revisión secundaria más detallada y completa, para llegar finalmente al inicio del tratamiento definitivo. Este proceso constituye el llamado ABCDE de la atención del trauma y permite identificar las situaciones que ponen en peligro la vida, cuando se sigue la siguiente frecuencia:41
A. Establecer una vía aérea definitiva con control de la columna cervical.
B. Resolver las lesiones torácicas graves que afectan la respiración y ventilación.
C. Reanimación inicial de líquidos y reposición de las pérdidas con previo control de la hemorragia.
D. Diagnóstico de déficit neurológico.
E. Exposición/ Control de ambiente: desvestir completamente al paciente previniendo la hipotermia.
La antibioticoterapia precoz, empírica y de amplio espectro iniciada en el preoperatorio es esencial para disminuir el riesgo de infecciones. Se utilizará una combinación de antibióticos que cubran gérmenes Gram negativos, aerobios, anaerobios y bacteroides por un plazo no menor a los 7 días; aunque recientes publicaciones sugieren que el empleo de monodroga y durante un período corto de tiempo tendría iguales resultados.3
Tratamiento quirúrgico
La vía de abordaje a la cavidad abdominal será a través de una incisión mediana. Se hará el diagnóstico de situación y se procederá a emplear alguna de las siguientes opciones terapéuticas para el manejo definitivo de las lesiones colónicas:
- Reparación primaria:
A. Cierre simple,
B. Resección colónica con anastomosis primaria.
- Colostomías:
A. Reparación primaria y colostomía proximal,
B. Resección colónica y exteriorización a cabos divorciados,
C. Resección colónica con exteriorización del cabo proximal y cierre del distal,
D. Exteriorización de la lesión como colostomía.
La asociación de hipotermia, acidosis y coagulopatía tienen implicancias negativas sobre el pronóstico; la vida del paciente depende de la posibilidad de superar el estado de shock con el menor daño residual quedando la resolución definitiva de la lesión colónica diferida al momento en que se considera que se ha recuperado la estabilidad hemodinámica (48-72 hs del tratamiento inicial). Se trata de traumatismos abdominales graves con lesiones multiviscerales y hemorragias exanguinantes en donde la lesión colónica es un componente más y no el más importante. He aquí donde el concepto de cirugía de “control del daño” toma relevancia, siendo una intervención quirúrgica en la cual se efectúan maniobras simples y rápidas para lograr el control de la hemorragia y de la pérdida de sustancias contaminantes (originadas por lesiones viscerales), seguidas de la finalización inmediata de la cirugía. Será factible en estos casos la resección del área colónica lesionada y la ligadura de los cabos distal y proximal, abandonándolos en la cavidad abdominal; difiriendo una eventual anastomosis en un segundo tiempo quirúrgico.42
En base al estado general del paciente y a los hallazgos en el intraoperatorio se decidirá que técnica quirúrgica será empleada. A continuación detallaré las principales consideración e indicaciones de cada una de ellas (graf. 6).43
Gráfico 6: Algoritmo terapéutico de las lesiones colónicas.
Reparación primaria
El cierre simple, en uno o dos planos con material absorbible, está indicado en las lesiones colónicas grado I de la Clasificación de Flint. Se deben recortar los bordes de las lesiones del colon producto de las heridas de arma de fuego debido al efecto lesional periorificial del proyectil.
La resección y anastomosis inmediata es apropiada en las lesiones colónicas grado II de la clasificación de Flint ubicadas en el colon derecho. La anastomosis puede hacerse en uno o dos planos con material absorbible.
Stone y Fabian44 establecieron los siguientes criterios de selección para los pacientes candidatos a un cierre primario:
- Ausencia de shock preoperatorio.
- Pérdida de sangre menor del 20% del valor normal estimado (menos de 1000 ml de sangre intraperitoneal).
- Lesión de no más de dos órganos intrabdominales.
- Mínima contaminación fecal.
- No deben haber transcurrido más de 8 horas entre el momento de la lesión y el acto operatorio.
- La pared colónica y la abdominal no deben tener una destrucción tisular que requiera resección.
Según las distintas series consultadas, la reparación primaria es un método seguro, con una morbimortalidad baja en comparación a la colostomía, si se realiza en pacientes seleccionados.
Colostomía
La reparación primaria con colostomía proximal está indicada en las lesiones grado I de la Clasificación de Flint ubicadas en el colon descendente, el sigma o el recto superior, cuando se hallan asociadas a otras lesiones proximales del colon transverso. Ésta última se exterioriza actuando como colostomía funcionante protegiendo el asa distal suturada. Siempre que se indica una colostomía proximal, es de utilidad lavar en el intraoperatorio el colon distal a la colostomía, con el fin de eliminar los restos de materia fecal en la luz colónica.
La resección colónica y exteririzacón a cabos divorciados o la exteriorización del cabo proximal y cierre del muñón distal se hallan indicadas en las lesiones grado III de la Clasificación de Flint. En las zonas móviles del colon, son sencillas las maniobras de exteriorización a cabos divorciados luego de la resección del segmento afectado. Cuando la resección no deja margen distal para la exteriorización, se lo resuelve con el cierre del muñón distal abocando el cabo proximal (Operación tipo Hartmann).
La exteriorización de la lesión como colostomía funcionante se indica en las lesiones grado II de la Clasificación de Flint ubicadas en el colon transverso o colon descendente. La exteriorización de la lesión es factible en todos los segmentos móviles del colon. Sin embargo, no es aconsejable para lesiones ubicadas en el colon derecho ya que el diámetro del cecoascendente y las características de su contenido fecal líquido hacen dificultoso el cuidado del ostoma. En ocasiones, por inestabilidad hemodinámica, contaminación fecal severa o por lesiones asociadas de otros órganos tales como el hígado, el páncreas o el duodeno o vasos como la vena cava o la arteria aorta, se requiere acortar el tiempo quirúrgico. Por lo tanto, la hemicolectomía derecha con abocamiento del cabo ileal y del cabo colónico es la táctica quirúrgica a emplear en las lesiones grado III de la Clasificación de Flint. Una alternativa es el abocamiento a distancia de la luz del ciego, mediante una sonda Pezzer, la cual se fija a la pared del colon mediante una doble jareta invaginante y al peritoneo parietal mediante puntos separados.
Stone y Fabian44 establecieron los siguientes criterios de selección para colostomía obligatoria:
- Shock preoperatorio grave.
- Hemoperitoneo de más de 1000 ml.
- Lesiones asociadas a más de dos órganos intrabdominales.
- Contaminación fecal importante.
- Tiempo de evolución entre el trauma y la intervención quirúrgica mayor de 8 hs.
- Destrucción de la pared colónica que requiera resección.
Pérdida de la pared abdominal.
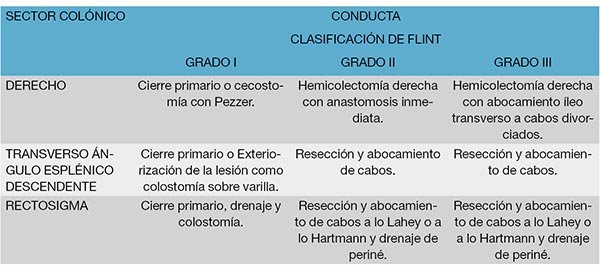
A modo de resumen se expondrá en la tabla 15 la conducta terapéutica que se debe emplear para la resolución de las lesiones del colon según la Clasificación de Flint y el sector colónico afectado.13, 14
El tratamiento no operatorio de las perforaciones colónicas por procedimientos endoscópicos fue descripto por primera vez en el año 1981.45 Es aplicable en pacientes en buen estado general, con preparación colónica suficiente y sin signos de peritonitis. Su tratamiento implica la supresión de la ingesta, la hidratación parenteral y la antibioticoterapia de amplio espectro. En caso de ser efectiva, los pacientes presentan buena evolución en las primeras 24hs. De lo contrario, se indicará la exploración quirúrgica.46 Dentro de las opciones terapéuticas se podrá realizar una reparación primaria con o sin colostomía de protección. La decisión depende del cirujano actuante de acuerdo a los hallazgos intraoperatorios.26 La primera publicación de una reparación exitosa de una perforación colonoscópica por medio de endoscopía fue en 1997.47 Como recaudo se debe insuflar el colon lo mínimo indispensable para evitar el derrame de materia fecal dentro de la cavidad y un posible síndrome compartimental abdominal por el neumoperitoneo hipertensivo.48 Por último, la reparación laparoscópica, gracias a sus nuevas técnicas y materiales de sutura, es cada vez más aceptada como opción para el manejo de las perforaciones colónicas. Bleier y col.49 llegaron a la conclusión que los pacientes operados por perforaciones colonoscópicas por vía laparoscópica tuvieron una evolución favorable, menos estadía hospitalaria, menor dolor postoperatorio, menor tamaño de incisiones, más rápida inclusión laboral y menor morbilidad.
Según Nelson y col.23 la mortalidad de las perforaciones por el colon por enema con bario es del 100% por lo que requiere un tratamiento quirúrgico precoz y agresivo, extremando los esfuerzos para extraer la mayor cantidad posible del bario derramado. Se deberá efectuar la resección del sector perforado con abocamiento de los cabos en forma divorciada. A fin de evitar este tipo de lesiones se recomienda sustituir el bario por contraste hidrosoluble y de postergar dichos estudios hasta pasada una semana después de la toma de una biopsia colónica.29
Tabla 15: Conducta terapéutica ante una lesión colónica en relación a su ubicación anatómica y la Clasificación de Flint
COMPLICACIONES
Las complicaciones de las lesiones traumáticas del colon se relacionan con el tipo y mecanismo lesional, el número y características de los órganos lesionados asociados, el grado de contaminación fecal, la estabilidad hemodinámica y la edad del paciente. La mayoría de las mismas son de tipo infeccioso: infección de la herida quirúrgica, absceso intrabdominal, dehiscencia de sutura y fístula enterocutánea.
Flint y col.17 refieren que las lesiones del colon derecho presentan un índice de complicaciones del 20% y una mortalidad del 9%. En las lesiones del colon transverso, las complicaciones fueron del 21% y la mortalidad, del 5%. En el caso de lesiones en el colon sigmoides las complicaciones fueron del 9% con una mortalidad del 3%. Según la Clasificación de Flint, las complicaciones fueron de 0% para las de grado I, 20% para las de grado II y de 31% para las de grado III.
George y col.31,33 hallaron un índice de complicaciones sépticas en las lesiones del colon que varían entre el 20 y el 60%. Reportan un índice de infección de la herida quirúrgica del 14% cuando se realizo el cierre simple, del 17% cuando se realizó la resección y anastomosis y del 29% cuando se efectuó una colostomía. La frecuencia de abscesos intrabdominales fue del 12%, 25% y 14% respectivamente.
Múltiples estudios demuestran que la incidencia de fístula postoperatoria es alrededor del 1,1 y el 6%.16,50-54
CONCLUSIONES
- Se evidenció en el último siglo una disminución en la morbimortalidad de las lesiones traumáticas del colon debido a la eficacia de la atención prehospitalaria y a la intervención quirúrgica temprana.
- Conocer las características anatómicas particulares que presenta el intestino grueso resulta trascendental para la exploración y tratamiento quirúrgico de las lesiones que involucran ha dicho órgano.
- La incidencia de las lesiones colónicas producto de los traumatismos de abdomen es variable; predominan los traumatismos penetrantes por proyectiles de baja energía, en hombres entre la segunda y cuarta década de la vida.
- Los traumatismos de abdomen con lesión colónica presentan sintomatología inespecífica. Se requiere de un alto índice de sospecha y la utilización de estudios complementarios para arribar al diagnóstico.
- El manejo inicial de todo paciente politraumatizado se hará en base a los protocolos de atención del ATLS propuesto por el Colegio Americano de Cirujanos.
- La inestabilidad hemodinámica, la evisceración, la proctorragia, la presencia de neumoperitoneo objetivado en la radiografía de tórax y la presencia de líquido libre en cavidad por medio de la ecografía abdominal son indicaciones de intervención quirúrgica de urgencia.
- La tomografía axial computada es el método de elección para el diagnóstico de lesiones asociadas. Requiere de la estabilidad hemodinámica del paciente para su realización.
- La laparoscopía detecta con exactitud la penetración a la cavidad abdominal siendo condición sine qua non para su uso que el paciente se encuentre estable hemodinamicamente.
- La rectosigmoideoscopía es de utilidad para el diagnostico de lesiones recto-colónicas producidas por cuerpos extraños introducidos a través del ano.
- La Clasificación de Flint tiene como ventajas su simplicidad y practicidad a la hora de optar cuál será la táctica quirúrgica ha emplear.
- La elección del tratamiento quirúrgico dependerá de la gravedad de la lesión colónica, el grado de contaminación fecal, las heridas asociadas y el estado general del paciente.
- La antibioticoterapia precoz, empírica y de amplio espectro es esencial para disminuir el riesgo de infecciones.
- La reparación primaria es un método seguro con una morbimortalidad baja, en comparación a la colostomía, si se realiza en pacientes seleccionados.
- La exteriorización de la lesión colónica como colostomía funcionante está indicada en lesiones grado II de la clasificación de Flint o bien en los casos en los cuales el estado hemodinámico del paciente no permite prolongar la cirugía.
- La reparación primaria y colostomía proximal está indicada en lesiones grado I de la clasificación de Flint ubicadas en el colon descendente, sigma y recto superior.
- La resección colónica y exteriorización a cabos divorciados o del cabo proximal está indicado en lesiones colónicas grado III de la clasificación de Flint.
- La inestabilidad hemodinámica asociada a la tríada de hipotermia, acidosis y coagulopatía en el contexto de lesiones colónicas graves, múltiples lesiones asociadas y hemorragias exanguinantes hace imperiosa la indicación de realizar cirugía de “Control del Daño”.
- Las complicaciones más frecuentes de las lesiones traumáticas del colon son las infecciosas.
- Las perforaciones iatrogénicas del colon por estudios endoscópicos pueden ser tratadas en forma no operatoria en pacientes con buen estado general, preparación colónica eficiente y sin signos de peritonitis.
- La resolución quirúrgica de las perforaciones endoscópicas puede ser llevada a cabo por vía minimamente invasiva en pacientes seleccionados y por cirujanos avezados, evidenciándose menores tasas de morbilidad en comparación a un abordaje abierto.
BIBLIOGRAFÍA
- Carpenter D, Bello J, Sokol T, et al.: The intracolonic by pass tube for left colon and rectal trauma. The Am Surgean, 1990, 56:769-771.
- Redcliffe A, Duddley H.: Intraoperative antegrade irrigation of the large intestine. SGO 1983, 156:721-723.
- Maxwell R, Fabian T.: Current management of colon trauma. World Journal of Surgery, 2003, 27:623-639.
- Stankovic N, Petrovic M.: Colon and rectal war injuries. The journal of Trauma, 1996, 40:183-188.
- Barredo C, Minetti A, Tisminetzky G.: Lesiones traumáticas del colon y recto. Rev Arg Coloproct, 1993, 5:38:42.
- Chappuis C, Frey D, Dietzen C, et al.: Management of penetrating colon injuries. Ann Surg, 1991, 213:492-498.
- Rouviere H, Delmas A.: Anatomía Humana Descriptiva, topográfica y funcional. 9ª edición, Barcelona, Masson, S.A., 1994, Tomo II, 409-435.
- Netter, F.: Atlas de Anatomía Humana. 6ª edición, Barcelona, Elsevier, Masson, 2015.
- Flores Nicolini F, Casaretto E.: Traumatismo de colon. Rev Arg Cirug, 1996:131-138.
- Abcarian H, Lowe R.: Colon and rectal trauma. Surgical Clinics of North America, 1978, 58:519-537.
- Torino F, Gimenez M, Moreno J.: Traumatismos penetrantes del abdomen por heridas de bala. Rev Arg Cirug, 1989,56:61-68.
- Garcia H, Andreani H, Gasali F, et al.: Traumatismos penetrantes del abdomen por heridas de bala: Un analisis de 400 casos. Premio Académico Diego E. Zavaleta, Facultad de Medicina, Universidad de Buenos Aires, 1996.
- Perera S, García H.: Cirugía de urgencia. 2ª edición. Buenos Aires. Médica Panamericana, 2005, 22:295-302.
- Dezanzo V, Pedro L.: Traumatismos de colon. Cirugía Digestiva. F. Galindo. www.sacd.org.ar, 2009, II-247,1-15.
- Burch J, Martin R.: Evolution of the Treatment of the Injured Colon in the 1980. Arch Surg, 1991, 126:979-984.
- Burch J.: Lesiones de colon y recto. En: Mattox K., Feliciano, Moore: Trauma, 2000, 4ª edición, 34:813-831.
- Flint L, Vitale G.:The Injured Colon. Relationships to management to complications. Ann Surg, 1981, 193:619-623.
- Barrizal J, Boyd D, Fol F, et al.: A critical review of management of 392 colonic and rectal injuries. Dis Col Rectum, 1974, 6:313-318.
- Vadra J.: Traumatismos de colon y recto. Casuística y resultados. Prensa Médica Argentina, 1993, 80:568-577.
- Faraoni H, Testa E.: Traumatismo del Colon. Revista Argentina de Cirugía, 1984, 46:50-57.
- Hebra A, Davidoff A, Ahmad S, et al.: Intestinal perforation due to an ingested foreign body: Laparoscopic management. J Laparo and Surg, 1996, 6:95-98.
- Velitchkov N, Grigorov G, Lasanoff J, et al.: Ingested foreign bodies of the gastrointestinal tract: retrospective analysis of 524 cases. World J. Surg 1996, 20:1001-1005.
- Nelson R, Alcarian H, Leela Prasad M.: Iatrogenic perforation of the colon and rectum. Dis Col Rectum, 1982, 25:305-308.
- Kavin H, Sinicrope F, Esker A.: Management of perforation of the colon at colonoscopy. Am J Gastroenterology, 1982, 87:161-167.
- Vincent M, Mcaninch J.: Management of perforation due to colonoscopy. Dis Col Rectum, 1983, 26:61-63.
- Lohsiriwat V, Sujarittanakarn S, Akaraviputh T, et al.: Colonoscopic perforation: A report from World Gastroenterology Organization endoscopy training center in Thailand. World J Gastroenterol, 2008, 14:67-225.
- Rathgaber S, Wick T.: Colonoscopy completion and complication rates in a community gastroenterology practice. Gastrointest Endosc, 2006, 64:556-62.
- Taku K, Sano Y, Fu KI, et al.: Iatrogenic perforation associated with therapeutic colonoscopy: a multicenter study in Japan. J Gastroenterol Hepatol, 2007, 2:1409-14.
- Fry R, Shemash E, Kodner U, et al.: Perforation of the rectum and sigmoid colon during barium enema examination. Dis Colon Rectum, 1989, 32:759-764.
- Barwick W, Schofftall R.: Routine exteriorization in the treatment of civilian colon injuries: a reappraisal. The American surgeon, 1978, 716.
- George S, Fabian T.: Primary repair of Colon Wounds. A prospective trial in nonselected patients. Ann Surg, 1989, 209:728-735.
- Ivatury R, Gaudino J.: Definitive Treatment of colon injuries: A prospective study. The American Surgeon, 1993, 59:43-49.
- George S, Fabian T.: Colon trauma: further support for primary repair. The American Journal of Surgery, 1988, 156:16-20.
- Ross S, Cobean R.: Blunt colonic injury: A multicenter review. The Journal of Trauma, 1992, 33:379-384.
- Alejandre S, Ballesteros M, Neira J.: Pautas de manejo definitivo del paciente traumatizado. Editorial Fundación Pedro Luis Rivero, Buenos Aires, 1996, 463-477.
- Moore E, Dunn E, Moore J, et al.: Penetrating abdominal trauma index. J Trauma, 1981, 21:439-45.
- Moore E, Cogbill T, Malangoni M, et al.: Organ injury scaling II: Pancreas, duodenum, small bowel, colon, and rectum. J Trauma, 1990, 30:14-279.
- Nelken N, Lewis F.: The influence or injury severity on complication rates after primary closure or colostomy for penetrating colon trauma. Ann Surg, 1989, 209:439-447.
- Huber P, Thal E.: Management of colon injuries. Surg Clin North Am, 1990, 70:561-573.
- Thompson J, Moore E.: Comparison of penetrating injuries of the right and left colon. Ann Surg, 1981, 88:414-418.
- Comité de trauma. Colegio Americano de Cirujanos. Soporte Vital Avanzado en Trauma (ATLS). 9ª edición, Chicago, 2012, 2-29.
- Gracia A, Reilly J.: Manual de Cirugía del Trauma. Traumatismos de colon. Comisión de Trauma. Asociación Argentina de Cirugía.
- Robert K.: Colon and Rectal Injuries. Dis Colon Rectum, 2006, 49:1203-1222.
- Stone H, Fabian T.: Management of perforating colon trauma. Ann. Surg., 1979, 190:430-436.
- Adair H, Hishon S.: The management of colonoscopic and sigmoidoscopic perforation of the large bowel. Br J Surg, 1981, 68:41-56.
- Lohsiriwat V.: Colonoscopic perforation: incidence, risk factors, management and outcome. World J Gastroenterol, 2010, 16:42-53.
- Yoshikane H, Hidano H, Sakakibara A, et al.: Endoscopic repair by clipping of iatrogenic colonic perforation. Gastrointest Endosc, 1997, 46:46-56.
- Fernandes M, Pires K, Chimelli P, et al.: Abdominal compartment syndrome during endoscopic clamping of an intestinal perforation secondary to colonoscopy. Rev Bras Anestesiol, 2009, 59:47-61.
- Bleier J, Moon V, Feingold D, et al.: Initial repair of iatrogenic colon perforation using laparoscopic methods. Surg Endosc, 2008, 22:646-649.
- Demetriades D, Murray J.: Penetrating colon injuries requiring resection: Diversion or primary anastomosis? An AAST prospective multicenter study. The Journal of Trauma, 2001, 50:765-775.
- Singer M, Nelson R.: Primary repair of penetrating colon injuries. A systematic review. Dis Colon Rectum, 2002, 45:1579-1587.
- Gonzalez R, Turk B.: Surgical options in colorectal injuries. Scand J Surg, 2002, 91:87-91.
- Won Jun Choi.: Management of Colorectal Trauma. J Korean Soc Coloproctol, 2011, 27:166-172.
- Zorcolo L, Covotta L, Carlomagno N, et al.: Safety of primary anastomosis in emergency colorectal surgery. Colorectal disease, 2003, Vol 5, 3:262-69
